Синдром Олбрайта — причины, диагностика и лечение. Псевдогипопаратиреоз (наследственная остеодистрофия Олбрайта): сложности дифференциально-диагностического поиска
Содержание
Страшный диагноз под названием синдром Олбрайта имеет неясную этиологию. Патология генетического происхождения проявляется повышенной пигментацией кожи и изменениями гормональной системы с ранним половым развитием. Редкое заболевание поражает весь организм человека. Многие больные страдают не только от физической отсталости, пациентам при болезни Олбрайта свойственна еще и умственная неполноценность.
Что такое синдром Олбрайта
Псевдогипопаратиреоз – так еще называют патологию, получившую название по фамилии американского ученого Фуллера Олбрайта (Fuller Albright) , открывшего это заболевание. Частота болезни встречается во всем мире как один случай на сто тысяч или на один миллион человек. Установить диагноз затруднительно, по этой причине болезнь Олбрайта может неверно распознаваться, что усложняет точное определение данных о ее распространенности.
Синдром Мак-Кьюна-Олбрайта (другой синоним патологии) развивается из-за генетических мутаций, которые начинают происходить в организме случайно, без обоснованных причин. Паращитовидная железа организма, регулирующая уровень кальция и фосфора, выделяет паратгормон. У заболевшего таким синдромом человека резистентность тканей к этому гормону нарушена. В итоге, костная система человека начинает разрушаться под действием результатов изменения метаболизма кальция и фосфора.
Для синдрома характерно появление на теле специфических пятен, фиброзной дисплазии и различных эндокринопатий . Среди последних самая частая – преждевременность полового развития. Редкой патологии подвержены как девочки, так и мальчики, но у лиц женского пола болезнь отмечается в два раза чаще. Отдельные генетики утверждают о подавляющей частоте больных среди девочек, так как характерный симптом раннего полового созревания у девочек отмечен почти в 10 раз чаще. Прочие проявления синдрома встречаются у обоих полов практически одинаково.
Причины
Этиология синдрома неизвестна. Предполагаются неврогенные влияния и эндокринные мутации, которые вызваны врожденными отклонениями в гипоталамической области при эмбриональном развитии и ранней продукцией гонадотропного гормона. Ученые считают, что развитие синдрома Мак-Кьюна-Олбрайта обуславливается отсутствием реакции клеток почек и костей на действие гормонов паращитовидных желез .
Уровень кальция и фосфора в кровеносной системе регулируется паращитовидными железами, но при этом патологическом состоянии их интактное (равнодушное) реагирование к колебаниям указанных элементов приводит к возникновению гиперпаратиреоза (избыточной продукции паратгормона), изменению структуры костей. В почках нарушается нормальный ход синтеза цАМФ – циклического аденозинмонофосфата, вспомогательного звена для распространения сигналов отдельных гормонов, в том числе паратгормона.
При синдроме Мак-Кьюна-Олбрайта сбой вызван мутацией генов . Нарушение может произойти в любом месте метаболической цепи: у кого-то поврежден рецептор, у ряда больных изменению подверглись белки мембраны клетки, у других наблюдается недостаточная продукция цАМФ. Связывающие эти случаи генетическая обусловленность не передается по наследству: мутация происходит уже после оплодотворения.

Симптоматика
Проявляющиеся признаки полностью обусловлены клеточным расположением мутировавшего гена. У некоторых пациентов диагноз подтверждается в раннем детстве, поскольку присутствуют явные аномалии в развитии костей и отмечается повышенная работа эндокринных желез (так, менструация может начаться в грудничковом возрасте – спорадические меноррагии). У других больных симптомы проявляются позже. Основные патологические признаки сопровождаются общим отставанием в развитии человека – интеллектуальном и физическом.
Болезнь Олбрайта характеризуется тремя главными признаками , при наличии двух из трех уже можно ставить этот диагноз:
- Преждевременное половое созревание. Симптом может проявляться в полной или неполной степени. Например, менструации начинаются очень рано, они обильны, болезненны, но при неполной форме симптома их может и не быть вовсе. В младенческом периоде появляются вторичные половые признаки, такие, как набухание и развитие молочных желез, часто появляются кисты на яичниках. У мальчиков же растут волосы на лобке и член.
- Фиброзная остеодисплазия. Рост скелета, его зрелость, окостенение значительно опережают стандартные показатели развития. Нарушение костной ткани ведет к искривлению костей, их деформации, характерна асимметричность. Самые частые признаки – хромота, искривление позвоночника. Рост замедляется, что заметно уже в детском возрасте, потом низкорослость начинает сопровождать еще и лишний вес. У многих больных происходит неравномерный рост черепа, возникает внешнее уродство, пучеглазие. В возрасте полового созревания изменения костей замедляются, количество переломов уменьшается.
- Изменения кожных покровов. Это проявляется в гиперпигментации. Кожный покров на туловище покрыт большими желто-коричневыми пятнами с неровными краями. Участки пигментации могут располагаться на пораженной стороне в области поясницы, на бедре, верхней части спины, ягодицах, груди. У ребенка светло-коричневые пятна появляются, как правило, сразу после рождения.
Диагностика
Болезнь Олбрайта трудно диагностируется у младенца, а в возрасте 6-10 лет симптоматика проявляется уже выраженно. Наблюдаются множественные отклонения в развитии костной системы, снижен кальций в крови, повышены фосфор и паратгормон. Больному назначаются анализы на гормоны (половые, тиреоидные, гонадотропин) . Чтобы подтвердить диагноз, проводится тест на уровень фосфатов и цАМФ, для чего в кровь больного вводится 200 единиц паратгормона и через четыре часа проводится анализ мочи.
Отсутствие повышения резистентности почек к паратгормону является достаточным основанием для постановки диагноза «болезнь Олбрайта». Проведение биохимического анализа крови, выявившего гипофосфатурию (недостаточное выведение фосфора с мочой), дополняется рентгенологическим исследованием для контроля изменения костей и мягких тканей. Женщины обязательно проходят осмотр у гинеколога, ультразвуковое исследование таза и анализ на половой хроматин. Очаги пятен бывают видны при рождении, но из-за небольшого размера и бледности их часто не замечают.

Лечение синдрома Олбрайта
Специфического лечения болезни Олбрайта нет, поскольку это результат генетической мутации. Лечение носит симптоматический характер , и начинать терапию требуется сразу же, поскольку промедление усугубляет умственную задержку. Больному назначают препараты кальция в суточных дозах, необходимых для поддержания нормальной концентрации минерала в организме, и прием витамина D в объеме до 100000 единиц в сутки: это кальцитриол, дигидротахистерол, оксидевит.
Для недопущения передозировки, уровень кальция и витамина D требует регулярного контроля. Чтобы не допустить преждевременной половой зрелости и для снижения эстрогена применяют гормональные препараты – антиандрогены, ингибиторы ароматазы. Для устранения проявления вторичного гиперпаратиреоза рекомендовано питание с пониженным содержанием фосфора.
Показанием для хирургического вмешательства являются прогрессирование нарушения зрительных функций, атрофия зрительного нерва. Для снятия болей применяют обезболивающие средства с небольшим количеством бисфосфонатов (веществ, предотвращающих потерю костной массы). При синдроме Мак-Кьюна-Олбрайта важно укреплять мускулатуру тела. Если терапия рациональна и начата вовремя, прогноз для жизни благоприятен. Женщина, страдающая такой патологией, решая завести детей, обязательно должна пройти обследование у генетика.
Фото людей с синдромом Олбрайта

Видео
Нашли в тексте ошибку?
Выделите её, нажмите Ctrl + Enter и мы всё исправим!
Болезнь Олбрайта – редко встречающаяся патология, которая формируется в костной системе и по своим симптомам схожа с . Характеризуется нарушением в кальциево-фосфорном обмене. В большинстве случаев отражается на развитии. В статье рассмотрим предпосылки, симптоматические проявления и особенности патологии.
Болезнь Олбрайта : особенности
Указанная патология является наследственной, была описана еще в 1942 г. врачом Олбрайтом.
Также название болезни связано с тем, что протекает с симптомами, характерными для гипопаратиреоза. Но в последнем случае причиной развития патологии является недостаток , возникающий при снижении активности ПЩЖ.
Псевдогипопаратиреоз провоцирует нарушение в чувствительности тканей на воздействие паратгормона, который содержится в достаточном количестве.
Как происходит регулирование паратиреоидного гормона, можно узнать из .
Начальный вариант патологии характеризуется:
- аномальным развитием скелета;
- резистентностью тканей (периферического типа) к паратгормону;
- гипокальциемией;
- клиническими симптомами, характерными для гипопаратиреоза.
Второй вариант характеризуется нормокальциемией и называется в медицине псевдопсевдогипопаратиреоз. В данном случае отсутствуют признаки гипокальциемии, гиперфосфатемии, а также судорожный синдром и остеомаляция.
Зафиксированы эпизоды наличия в семье двух вариантов развития болезни: гипо- и нормокальциемических. Возможен переход болезни из одной формы в другую.

Ложный гипопаратиреоз : причины

Несмотря на то, какой вариант болезни у человека, она будет наследственной, наследование – аутосомно-доминантное, сцепление происходит с Х-хромосомой.
При проведении исследования родословных, выявлено, что количество пациенток женского пола встречается чаще, чем мужского. Также стоит отметить, что патология не передается от отца – к сыну .
Объяснить развитие болезни Олбрайта можно наличием генетической резистентности, которая отмечается в почках и скелете, к воздействию на них паратгормона. Это объясняется наличием дефекта в рецепторах клеток-рецепторов, а также реабсорбцией фосфора. При нарушении выведения микроэлемента с мочой, может развиться гиперфосфатемия и гипокальциемия (чаще всего вторичная).
ПЩЖ при наличии патологии – интактна, поэтому гипокальциемия способна привести к стимуляции синтеза паратгормона и развитию .
Псевдогипопаратиреоз провоцирует:
- компенсаторную гиперплазию ПЩЖ;
- нарушения в костной ткани (кисты, остеопороз);
- отложения кальцинатов, которые формируются в почках, артериях, скелетных мышцах, миокарде, роговице и конъюнктиве глаза, а также в клетчатке (подкожной).
При болезни Олбрайта часто диагностируются и другие патологии, например, СД, артериит, полиартрит, гипертензия (артериальная).

Симптоматика
Клиника болезни схожа с такими же при гипопаратиреозе (идиопатического типа).
Эндокринные проявления:
- низкий рост;
- избыточный вес;
- лицо луноподобного вида;
- олигоменорея.

Может сочетаться с эндокринными патологиями:
- гинекомастией.
Неврологические проявления выражаются в тонических судорогах, возникающих приступообразно и спонтанно. Происходить это может при наличии раздражителей любого вида.
Для пациентов характерен недостаточный рост, чаще всего отмечается отставание в физическом и умственном формировании.

Определение
Патология определяется у 5-10-летних детей, также учитывается характерная симптоматика, рентген и показатели проведенные лабораторных исследований.
В большинстве случаев выявляется:
- гипокальциемия;
- гиперфосфатемия;
- отклонение активности фосфатазы (щелочного вида);
- рост концентрации паратгормона;
- снижение вывода фосфора и кальция.

При помощи теста, выявляющего число выведенных с мочой фосфатов, можно определить нечувствительность канальцев почек к паратгормону.
При введении его внутривенно, повышение уровня фосфатов не происходит.
Во время проведения рентгенографии (чаще всего изучается состояние суставов и костей), определяются изменения, сформированные в костной ткани. Чтобы исключить наличие в других органах возможных поражений, а также для проведения дифференциальной диагностики, потребуется консультация у специалистов: эндокринолога, офтальмолога, а также невролога. Женщинам рекомендуется также посетить и гинеколога, а мужчинам – уролога.
При необходимости, в качестве дополнительного обследования, проводят , мочевого пузыря, почек, а также ЭКГ, ЭЭГ, офтальмоскопию.
Терапия
Основное направление лечения – выполнить коррекцию гипокальциемии. Для этих целей назначаются кальциесодержащие препараты.
Catad_tema Педиатрия - статьи
Псевдогипопаратиреоз (наследственная остеодистрофия Олбрайта): сложности дифференциально-диагностического поиска. Клиническое наблюдение
Е.В. Тозлиян, педиатр-эндокринолог, генетик, к. м. н., И.В. Шулякова, невролог, к. м. н.,
обособленное структурное подразделение «Научно-исследовательский клинический институт педиатрии» ГБОУ ВПО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Минздрава РФ, г. Москва
Ключевые слова:
дети, псевдогипопаратиреоз, наследственная остеодистрофия Олбрайта, ожирение, гипокальциемия, диагностика, резистентность к паратиреоидному гормону.
Keywords:
children, pseudohypoparathyroidism, Albright hereditary osteodystrophy, obesity, hypocalcemia, diagnostics, parathyroid hormone resistance.
Псевдогипопаратиреоз (греч. pseudes – ложный + гипопаратиреоз; синоним: наследственная остеодистрофия Олбрайта, синдром «яванской курицы») – редкое наследственное заболевание костной системы, имитирующее гипопаратиреоз и характеризующееся нарушением обмена кальция и фосфора; часто сопровождается задержкой умственного и физического развития. Заболевание описано впервые американским врачом-эндокринологом Albright F. в 1942 году . Распространенность заболевания составляет 7,9 на 1 млн человек .
ГЕНЕТИЧЕСКИЕ ДАННЫЕ
Псевдогипопаратиреоз (ПГП) – генетически гетерогенное заболевание. Данные о типе наследственной передачи противоречивы: как X-сцепленный доминантный , так и аутосомно-доминантный, аутосомно-рецессивный типы . В большинстве случаев развитие наследственной остеодистрофии Олбрайта связано с мутациями в расположенном на хромосоме 20 локусе 20q13 гена GNAS1 (Patten et al., 1990), кодирующего белок Gs-альфа, связанного с рецептором паратиреоидного гормона (ПТГ) . Подобный фенотип выявлен и у больных с интерстициальной делецией длинного плеча хромосомы 2 локуса 2q37 .
ПАТОГЕНЕЗ
В основе патогенеза псевдогипопаратиреоза лежит генетически обусловленная резистентность почек и скелета к действию парат-гормона в результате дефекта комплекса «специфический циторецептор – паратгормон – аденилатциклаза», что нарушает процесс образования в почках циклического 3"-, 5"-аденозинмонофосфата (цАМФ), являющегося внутриклеточным посредником действия паратгормона на метаболические процессы. Псевдогипопаратиреоз является генетически гетерогенным заболеванием. У части больных дефектен сам циторецептор, связывающий паратгормон (тип 1А псевдогипопаратиреоза), у других отмечается дефект нуклеотидсвязывающего белка, локализованного в липидном бислое клеточной мембраны и функционально связывающего рецептор с аденилатциклазой (тип 1B псевдогипопаратиреоза). У некоторых больных наблюдается ферментативная недостаточность самой аденилатциклазы (псевдогипопаратиреоз 2-го типа). Дефицит цАМФ, получающийся вследствие этих дефектов, ведет к нарушению синтеза специфических белков, определяющих биологический эффект паратгормона. Таким образом, теряется чувствительность органов-мишеней к паратгормону .
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА
В настоящее время выделяют 4 клинические формы патологии: типы 1А, 1В, 1С и 2. Знание их клинико-биохимических особенностей и данных генетических исследований позволяет провести дифференциальную диагностику в рамках самой нозологической формы.
Общими признаками, позволяющими заподозрить заболевание, являются диспропорциональность физического развития, низкий рост (до карликовости) за счет укорочения нижних конечностей (фото 1), брахидактилия (фото 2), круглое «лунообразное» лицо (фото 3). Иногда наблюдаются экзостозы и аплазия зубов.
Фото 1.
Внешний вид ребенка с остеодистрофией Олбрайта
(особенности фенотипа, низкий рост за счет укорочения нижних конечностей)
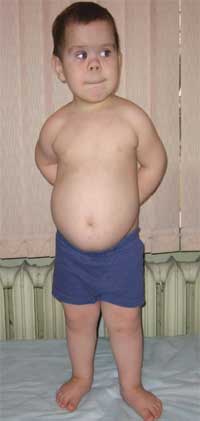
Фото 2.
Особенности костной системы у больного
с остеодистрофией Олбрайта
(брахидактилия – укорочение пальцев)

Фото 3.
Особенности фенотипа ребенка
с остеодистрофией Олбрайта
(круглое «лунообразное» лицо)

Патогномоничным признаком считается резкое укорочение I, III и V пястных и плюсневых костей (особенно III и IV), вследствие чего II пальцы на кистях и стопах оказываются длиннее остальных, а при сжатии кисти в кулак отсутствуют выпуклости в области IV и V пястно-фаланговых суставов – так называемый брахиметафалангизм. Выявляются также короткие широкие фаланги, утолщение свода черепа и деминерализация костей (остеопороз), ожирение .
Умственная отсталость (чаще умеренной степени выраженности) обнаруживается примерно у 20% больных. По данным некоторых авторов , олигофрения встречается в 70% случаев при наличии гипокальциемии и в 30% случае при нормокальциемии. Психические процессы у больных замедлены. В неврологическом статусе нередко отмечаются моторная неловкость, невротические реакции: страхи, тревога, беспокойство, плохой сон, повышение рефлексов, судороги, носящие тетанический характер и обусловленные гипокальциемией, иногда судорожные пароксизмы. Описаны также миопатические симптомы: мышечная утомляемость, мышечная слабость. Часто наблюдаются экстрапирамидные нарушения: хореиформные гиперкинезы, атетоз, лицевой гемиспазм, паркинсонизм, в отдельных случаях имеют место эпилептические пароксизмы, мозжечковые симптомы: атаксия, нарушение координации.
Нередко определяются кальцификация мягких тканей, подкожные кальцификаты (грудь, живот, пяточные сухожилия), при гистологическом исследовании которых – osteoma cutis (Izraeli et al., 1992), мозге (базальные ганглии). Важно отметить, что кальцификаты могут быть уже при рождении. Вследствие гипокальциемии обычно развивается катаракта и возникают дефекты эмали зубов.
ПСЕВДОГИПОПАРАТИРЕОЗ ТИПА 1А
имеет аутосомно-доминантный тип наследования. Ген псевдогипопаратиреоза типа 1А – GNAS1 – локализован на длинном плече хромосомы 20, в локусе 20q13.2. Развитие заболевания связано с дефицитом гуанин-нуклеотид-связывающего белка (Gs-белок). При этом ПТГ, связываясь с рецепторами тканей-мишеней, не способен активизировать циклический аденозинмонофосфат (цАМФ) и вызвать тканевой ответ. Вероятно, подобный механизм лежит в основе развития нечувствительности тканей других органов и эндокринных желез (гипофункция щитовидной железы, гонад, гипофиза, сахарный диабет, а также сниженный ответ печени на введение глюкагона), наблюдаемой при псевдогипопаратиреозе типа 1А. При данном типе патологии не наблюдается характерной для нормы повышенной экскреции цАМФ с мочой в ответ на экзогенное введение ПТГ. Заболевание диагностируется чаще в возрасте 5–10 лет. У больных наблюдаются низкий рост, короткая шея, круглое лицо, укорочение метакарпальных и метатарзальных костей (чаще укорочение IV и реже II пальцев) – так называемый брахи-метафалангизм. Отмечаются кальцификация мягких тканей, подкожные кальцификаты, которые могут выявляться уже при рождении; нередко наблюдается одновременное вовлечение других эндокринных желез: щитовидной железы (гипофункция), гонад, поджелудочной железы (сахарный диабет). Вследствие гипокальциемии нередко развиваются катаракта и дефект эмали зубов. В качестве дифференциально-диагностического теста отличия ПГП типа 1А от гипопаратиреоза: отсутствие клинического эффекта от парентерального введения ПТГ в виде подъема уровня кальция в крови и увеличения почечной экскреции фосфора с мочой (фосфатурический эффект).
При биохимическом исследовании выявляются гипокальциемия, гиперфосфатемия, увеличение уровня паратиреоидного гормона в крови, гипофосфатурия. Уровень Gs-белка в крови снижен. При рентгенологическом исследовании костной системы обнаруживаются укорочение метакарпальных и метатарзальных костей, генерализованная деминерализация, утолщение костей свода черепа.
ПСЕВДОГИПОПАРАТИРЕОЗ ТИПА 1B
имеет аутосомно-доминантный тип наследования, однако не исключен доминантный, сцепленный с Х-хромосомой тип наследования. Необходимо иметь в виду наблюдающуюся иногда неполную пенетрантность гена болезни и возможность скрытого носительства патологии. Поэтому рекомендуется клиническое (выявление субклинического течения болезни) и биохимическое обследование (определение уровней кальция, фосфора, ПТГ крови) предполагаемых носителей заболевания. ПГП типа 1В обусловлен дефицитом тканевых рецепторов к паратиреоидному гормону в органах-мишенях и ограниченной резистентностью к паратгормону. Клиническая картина сходна с клиникой типа 1А, но отсутствует поражение других эндокринных желез, реже встречается остеодистрофия.
У больных отсутствует реакция почек на экзогенное введение паратиреоидного гормона в виде увеличения экскреции циклического аденозинмонофосфата с мочой, однако, в отличие от типа 1А, уровень Gs-белка в крови нормален. Женщины поражаются чаще мужчин, однако тяжесть заболевания может быть одинаковой как у мужчин, так и у женщин.
ПСЕВДОГИПОПАРАТИРЕОЗ ТИПА 1С
некоторые авторы отождествляют с псевдо-псевдогипопаратиреозом (ППГП), описанным Albright F. в 1952 году. Характеризуется свойственной ПГП клинической картиной, однако уровни кальция, фосфора в крови и моче остаются в пределах нормы. Показатели ПТГ и Gs-белка в крови также сохраняются на нормальном уровне. У некоторых больных с ПГП типа 1С обнаруживаются делеции de novo на хромосоме 2 . Не исключено, что этот вариант болезни является подтипом ПГП типа 1А.
ПСЕВДОГИПОПАРАТИРЕОЗ ТИПА 2
клинически сходен с другими типами заболевания, однако имеет аутосомно-рецессивный тип наследования. Не исключено существование и аутосомно-доминантных форм патологии. Патогенез развития связан с внутриклеточной резистентностью к цАМФ. ПТГ при этом связывается с рецепторами и вызывает нормальную ответную реакцию клеток на ПТГ в виде увеличения экскреции цАМФ. Внутриклеточная нечувствительность к цАМФ, однако, не позволяет осуществиться полной реализации действия ПТГ. При этом сохраняется нормальная реакция почек на экзогенное введение паратиреоидного гормона в виде увеличения экскреции циклического аденозинмонофосфата с мочой. Высказывается мнение, что ПГП типа 2 может быть связан с дефицитом витамина D .
Таким образом, выделенные типы ПГП клинически характеризуются пониженной чувствительностью органов-мишеней к ПТГ, однако различаются патогенетическими механизмами формирования нечувствительности тканей.
ДИАГНОСТИКА
Лабораторным дифференциально-диагностическим тестом может служить характер почечной экскреции цАМФ в ответ на введение ПТГ: повышенная экскреция цАМФ отмечается при типе 2 и ее отсутствие – при типе 1. Диагноз подтверждается обнаружением сниженного уровня гуанин-нуклеотидсвязывающего белка (Gs-белок) в крови (в среднем в 1,5–2 раза) по сравнению с нормой. Гипокальциемия, как правило, сочетается с гиперфосфатемией и гипофосфатурией. Уровень ПТГ повышен; при 1C-типе уровень ПТГ в норме, что дало основание для названия «псевдогипопаратиреоз». При рентгенологическом исследовании костной системы обнаруживаются укорочение пястных и плюсневых костей, нередко генерализованная деминерализация (остеопороз), утолщение костей свода черепа. В дерматоглифическом рисунке отмечается смещение осевого ладонного трирадиуса.
Критерии диагноза:
- низкий рост;
- круглое лицо;
- задержка нервно-психического развития;
- скелетные аномалии;
- низкое содержание кальция в сыворотке крови;
- высокий уровень паратиреоидного гормона в крови;
- снижение экскреции с мочой фосфатов и цАМФ.
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА
Лечение при гипокальциемии заключается в назначении препаратов кальция в дозах, достаточных для поддержания нормальной концентрации кальция в крови. Большое значение имеет терапия витамином D. В настоящее время применяют активные метаболиты витамина D – оксидевит, 1-альфа-Д3, кальцитрин и др. в дозе 1–2 мкг/сутки с положительным результатом (увеличение содержание кальция в крови, уменьшение проявлений судорожного синдрома). Эффективен также тахистин (0,5–1,5 мг/сутки). Данный препарат увеличивает всасывание кальция в кишечнике и тем самым способствует повышению уровня кальция в крови. Противосудорожная терапия используется как дополнительное лечение. На интеллектуальное развитие лечение не оказывает заметного действия, но наряду с уменьшением симптомов судорожного синдрома наблюдается регресс неврологических проявлений (подкорковых нарушений, хореиформных гиперкинезов, атетоза и др.). Во избежание передозировки препаратов витамина D необходим контроль концентрации кальция в крови каждые 3–7 дней в течение первых 2 недель лечения и каждый месяц в течение последующих 2–3 месяцев. По достижении стабильной концентрации кальция в крови достаточно проверять ее 1 раз в 2–3 месяца. Диета с ограничением фосфора помогает нормализовать как концентрацию фосфора, так и содержание кальция в крови и устранить симптомы вторичного гиперпаратиреоза. При недостаточности других желез внутренней секреции проводят заместительную терапию соответствующими гормонами.
Лечение паратгормоном неэффективно. Для купирования судорожных приступов внутривенно вводят 10%-ный раствор кальция хлорида или кальция глюконата; внутрь – 5–10%-ный раствор кальция хлорида по 1 столовой ложке 3–4 раза в день: кальция глюконат, кальция лактат – до 10 г в день.
ПРОГНОЗ для жизни определяется выраженностью судорожного синдрома.
ПРОФИЛАКТИКА болезни основывается на данных медико-генетического консультирования.
МЕДИКО-ГЕНЕТИЧЕСКОЕ КОНСУЛЬТИРОВАНИЕ
При медико-генетическом консультировании следует исходить из аутосомно-доминантного типа наследования и высокого (50%) риска повторения заболевания в семье при унаследованных формах. С целью идентификации характера типа наследования необходимо проводить тщательное обследование родителей, так как синдром может проявляться минимальными клиническими симптомами. В настоящее время разработана и совершенствуется молекулярно-генетическая диагностика заболевания путем типирования мутаций в гене GNAS1 на хромосоме 20. Разрабатываются способы пренатальной диагностики заболевания в целом и отдельных его типов.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ Мальчик Г., 14,5 лет (фото 4), поступил в Научно-исследовательский клинический институт педиатрии с диагнозом: дегенеративное заболевание нервной системы? врожденная наружная гидроцефалия; симптоматическая эпилепсия; наследственный синдром? болезнь накопления? метаболическая энцефалопатия; субклинический гипотиреоз; низкорослость смешанного генеза; когнитивные нарушения.
Жалобы при поступлении на интенсивные приступообразные головные боли, локализующиеся в лобной области и сопровождающиеся рвотой, которая приносит облегчение, снижение памяти и успеваемости в школе, судорожные приступы, во время которых происходит подергивания в правой руке.
Фото 4.
Ребенок Г., 14,5 лет, с остеодистрофией Олбрайта
(особенности фенотипа, низкий рост, укорочение конечностей, брахидактилия)

Анамнез семейный: родители – армяне по национальности, не состоящие в кровном родстве и не имеющие профессиональных вредностей. В родословной случаев психических заболеваний, эпилепсии, задержки в развитии – не отмечалось. Сибс, сестра 17 лет – со слов – здорова.
Анамнез жизни и заболевания:
мальчик от 2-й беременности, протекавшей без особенностей, роды вторые, в срок, физиологические, масса при рождении – 3100 г, длина – 51 см. Закричал сразу, оценка по шкале Апгар – 7/9 баллов. Ухудшение состояния на 3-и сутки – судороги неонатальные, купированы в роддоме. Ранний постнатальный период – без особенностей. Отмечалась незначительная темповая задержка моторного развития на первом году жизни, самостоятельная ходьба с 1 года 3 мес. В связи с чем наблюдался неврологом с диагнозом: органическое поражение ЦНС; врожденная гидроцефалия; неонатальные судороги; фебрильные судороги в анамнезе.
Получал диакарб, финлепсин. Дебют приступов с 1 года 11 мес. – асимметричные, тонические в виде напряжения правой руки и ноги, с заведением глаз, до 2 мин., без потери сознания, частые до 10 эпизодов в сутки. Получал депакин нерегулярно. На фоне самостоятельной отмены – однократный тонический статус. В 2 года проведена по месту жительства КТ головного мозга, где выявлены единичные очаги демиелинизации в затылочных долях.
Консультирован нейрохирургом, рекомендовано консервативное лечение. С 3 лет отмечается задержка психоречевого развития, рекомендовано наблюдение психиатра.
С 4–5 лет родители стали отмечать деформацию и укорочение пальцев стоп и кистей, в особенности II–IV пальцев симметрично на руках и ногах, снижение ростовых показателей. В 8 лет заключение логопеда – общее нарушение речи 2–3-го уровня, рекомендовано обучение в специализированной школе. В этом же возрасте осмотр генетиком по месту жительства, заключение: наследственная болезнь обмена? рекомендовано исследование аминокислот крови, изменений не было выявлено; окончательное заключение: данных за наследственное заболевание обмена не выявлено; гипохондроплазия; рекомендовано лечение невролога и эндокринолога.
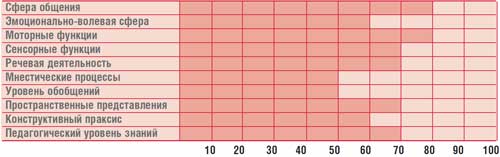
Таблица.
Профиль психического развития ребенка Г., 14,5 лет (IQ = 68)
В возрасте 8 лет консультирован эндокринологом по поводу задержки роста и развития. При рентгенологическом исследовании кистей рук отмечены особенности: средние, основные фаланги и пястные кости укорочены, утолщены; диагноз рентгенолога – ахондроплазия.
Неоднократно обследуется по месту жительства в неврологическом стационаре. В 12 лет появились судорожные приступы без потери сознания с подергиванием правой руки, носящие серийный характер, назначена противосудорожная терапия (депакин), частота приступов значительно сократилась. В 13 лет проведена МРТ головного мозга с контрастированием – симметричные изменения в основании височных долей на уровне ядер в виде повышения МР-сигнала, что характерно для токсических (марганец) или метаболических (медь, железо) энцефалопатий.
Вновь осмотрен в возрасте 13 лет 3 мес. эндокринологом, при исследовании тиреоидного профиля выявлено повышение тиреотропного гормона (ТТГ), диагностирован субклинический гипотиреоз, назначен L-тироксин.
При анализе амбулаторной карты ребенка и документации по месту жительства исследование кальция и фосфора проводилось однократно, в возрасте 1,5 лет, отмечалась гипокальциемия, но по данному поводу дообследование не проводилось. Учитывая неопределенность диагноза по месту жительства, генетиком ребенок направлен в Москву, в Научно-исследовательский клинический институт педиатрии, с целью уточнения диагноза.
Данные объективного исследования:
Рост – 143 см, масса – 43 кг.
Физическое развитие очень низкое, гармоничное, телосложение диспропорциональное за счет укорочения конечностей. Sds роста соответствует –2,8 отклонениям от нормы (норма –2+2).
Особенности фенотипа: круглое лицо, короткая шея, антимонголоидный разрез глазных щелей, широкое переносье, высокий лоб, брахидактилия, укорочение IV и V пястных и плюсневых костей (фото 5). По внутренним органам – без особенностей. Половое развитие – Tanner III–IV стадия (что соответствует возрасту).
Данные лабораторных и функциональных исследований:
Клинический анализ крови и мочи – норма.
Биохимический анализ крови: общий кальций – 1,39 (норма 2,02–2,6 ммоль/л), кальций ионизированный – 0,61 (норма 1,13–1,32 ммоль/л), фосфор неорганический – 3,66 (норма 0,86–1,56 ммоль/л), остальные показатели в пределах нормы.
Биохимический анализ мочи: почечная экскреция фосфатов снижена – 11,5 ммоль/л (норма 19–32 ммоль/л).
Тиреоидный профиль: ТТГ – 11,75 (норма 0,4–4,0 мкМЕ/мл), свободный Т4 – 0,49 (норма 1,0–1,8 нг/дл).
Паратиреоидный гормон – 499 (норма 12– 65 пг/мл), СТГ – 7 нг/мл (норма 7–10 нг/мл), соматомедин-С – 250 нг/мл (норма 88–360 нг/мл).
УЗИ внутренних органов – без особенностей.
ЭКГ – миграция суправентрикулярного водителя ритма на фоне регулярной ЧСС 71– 80 уд/мин. Неполная блокада правой ножки пучка Гиса. Нарушение процесса реполяризации в миокарде задней стенки левого желудочка (снижение з.Т III, аVF).
R-графия позвоночника – правосторонний сколиоз грудного отдела позвоночника 1-й степени, выраженный остеопороз.
R-графия кистей рук с захватом предплечий – укорочение и расширение концевых и средних фаланг. Костный возраст – 13,5– 14 лет.
ЭЭГ-паттернов эпилептической активности не зарегистрировано.
МРТ головного мозга – МР-картина множественных субкортикальных очагов повышенного МР-сигнала в лобных долях, наружная компенсированная гидроцефалия с атрофией вещества головного мозга.
МСКТ головного мозга – симметричные участки обызвествления лентиформных ядер. Диффузные гиперденсивные участки в таламусах, хвостатых ядрах с участком обызвествления справа. Множественные точечные обызвествления покровных мягких тканей черепа.
Аудиограмма – без патологии.
ДНК-диагностика в гене GNAS1 – в работе.
Консультации специалистов:
Эндокринолог – наследственная остеодис-трофия Олбрайта типа 1А (псевдогипопара-тиреоз). Первичный гипотиреоз, неполная медикаментозная компенсация.
Окулист – катаракта полная вторичная. Рекомендовано оперативное лечение.
Психолог – когнитивные нарушения (психологический профиль ребенка представлен в табл.).
Учитывая фенотип ребенка, данные анамнеза, результаты дополнительных исследований (гипокальциемия, гиперфосфатемия, гипофосфатурия, повышение паратиреоидного гормона крови), кальцинаты в веществе головного мозга, наличие катаракты, гипотиреоза), поставлен диагноз: наследственная остеодистрофия Олбрайта 1А-типа (псевдогипопаратиреоз). Рекомендовано проведение ДНК-диагностики - поиск мутаций в гене GNAS1.
Лечение: ребенку рекомендован прием эутирокса в дозе 100 мкг/сутки; активный метаболит витамина Д - альфа-Д3 («Тева») в дозе 2 мкг/сутки; кальций («Сандоз») 2000 мг/сутки; постоянный прием противосудорожной терапии - финлепсин 800 мг/сутки под наблюдением невролога-эпилептолога; занятия с логопедом-дефектологом и психологом; энерготропная терапия (Элькар и коэнзим Q10 в возрастных дозах). Контроль показателей фосфорно-кальциевого обмена, уровня паратгормона.
Таким образом,
представленное клиническое наблюдение демонстрирует сложности дифференциально-диагностического поиска, важность своевременного исследования простых биохимических параметров (при эпилепсии обязателен неоднократный скрининг показателей фосфорно-кальциевого обмена), исходы поздней диагностики генетически детерминированного заболевания, необходимость интегрировать отдельные признаки в общий фенотип того или иного патологического состояния для целенаправленной своевременной диагностики отдельных форм наследственных заболеваний. Своевременная диагностика, уточнение генеза каждого синдрома особенно важны, так как позволяют найти оптимальный подход к лечению этих состояний, профилактике возможных осложнений (вплоть до инвалидности ребенка); предупреждение повторного возникновения наследственных болезней в пораженных семьях (медико-генетическое консультирование). Это диктует необходимость врачам различных специальностей четко ориентироваться в потоке наследственно обусловленной патологии. Список литературы находится в редакции.
Синдром Мак-Кьюна-Олбрайта был назван в честь двух выдающихся врачей, описавших его более полувека назад. Они рассказали обществу о детях, большинство из которых были девочками. У многих из них был низкий рост, круглое лицо, короткая шея, укороченные IV и V плюсневые или пястные кости, имели место спазмы мышц, изменение скелета, задержка прорезывания зубов, гипоплазия эмали. Наблюдалась также задержка умственного развития и эндокринные заболевания, выраженные ранним половым созреванием с менструальным кровотечением, развитием груди, ростом волос на лобке и груди, увеличением темпов роста детей и изменением кожи.
В современной медицине термин «синдром Олбрайта» используется применительно к пациентам, имеющим все или лишь некоторые эндокринные и кожные аномалии. Есть случаи, когда диагноз ставили в раннем детстве. Однако в типичных случаях его ставят детям в 5-10 лет, на основании признаков, которые свойственны этому заболеванию. Вообще оно является редким и передается по наследству. Остаются неизвестными как этиология, так и патогенез этого недуга.
Причины синдрома
Этиология синдрома неизвестна. Предполагаются неврогенные влияния и эндокринные мутации, которые вызваны врожденными отклонениями в гипоталамической области при эмбриональном развитии и ранней продукцией гонадотропного гормона. Ученые считают, что развитие синдрома Мак-Кьюна-Олбрайта обуславливается отсутствием реакции клеток почек и костей на действие гормонов паращитовидных желез.
Уровень кальция и фосфора в кровеносной системе регулируется паращитовидными железами, но при этом патологическом состоянии их интактное (равнодушное) реагирование к колебаниям указанных элементов приводит к возникновению гиперпаратиреоза (избыточной продукции паратгормона), изменению структуры костей. В почках нарушается нормальный ход синтеза цАМФ – циклического аденозинмонофосфата, вспомогательного звена для распространения сигналов отдельных гормонов, в том числе паратгормона.
При синдроме Мак-Кьюна-Олбрайта сбой вызван мутацией генов. Нарушение может произойти в любом месте метаболической цепи: у кого-то поврежден рецептор, у ряда больных изменению подверглись белки мембраны клетки, у других наблюдается недостаточная продукция цАМФ. Связывающие эти случаи генетическая обусловленность не передается по наследству: мутация происходит уже после оплодотворения.
Симптоматика
Характерными видимыми признаками можно назвать:
- низкий рост;
- излишний вес;
- высокий уровень глюкозы;
- лунообразное лицо;
- нарушения полового созревания.
Могут проявляться и следующие симптомы:
- акромегалия;
- аутоиммунные заболевания;
- гинекомастия;
- болезнь Иценко-Кушинга и др.
Больные часто жалуются на кровь в моче, постоянную рвоту, изменения в зубах, судороги. При осмотре видна подкожная оссификация, при чем кальцинаты могут изъявляться.
Часто у больных укорочены пальцы, деформируются эпифизы трубчатых костей, могут быть признаки лентикулярной катаракты.
Почти всегда такие больные отстают в умственном развитии.
Диагностика заболевания
При диагностировании заболевания проводятся следующие исследования:
- Описываются клинические проявления;
- Больного с синдромом олбрайта направляют на обследование к генетику;
- Рентгенологическое исследование;
- Анализы на гормоны (половые, тиреоидные, гонадотропин и прочие по показаниям);
- Ультразвуковое исследование таза;
- Обследование у эндокринолога, гинеколога (для девочек), уролога (для мальчиков);
При необходимости исследование органов эндокринной системы.
Люди с заболеванием синдром олбрайта стоят на учете у нескольких специалистов, в наблюдении которых нуждаются (гинеколог – эндокринолог, специалист по лучевой диагностики, ортопед-травматолог). Кроме посещения врачей, пациентам необходимо периодически сдавать анализы на гормоны (тропные, гонадотропный).
Лечение патологии
Синдром Олбрайта - неизлечимое заболевание. Для поддержания жизни больных на оптимальном уровне и устранения основных клинических признаков болезни проводят симптоматическую терапию. Если общетерапевтические мероприятия не будут проведены вовремя, задержка умственного развития только усугубится.
Индивидуально разработанная диетотерапия со сниженным содержанием фосфора в рационе способствует формированию нормального уровня кальция в крови.
Комплексное лечение проявлений синдрома включает:
- препараты кальция - «Кальций Д3 Никомед», «Кальцемин», «Кальцемин Адванс»;
- препараты, связывающие фосфор и замедляющие его всасывание кишечником - «Ацетат кальция», «Нефросорб», «Ренацет»;
- средства, содержащие витамин Д - «Кальцитонин», «Миакальцик», «Сибакальцин»;
- антиандрогены - «Диане-35», «Жанин», «Ярина»;
- препараты прогестерона - «Утрожестан», «Дюфастон»;
- лекарства, подавляющие синтез гормонов щитовидной железы - «Тиамазол», «Мерказолил»;
- средства, уменьшающие синтез кортизола - «Бромкриптин», «Трилостан», «Митотан»;
- препараты, подавляющие выработку гормона роста - «Соматулин», «Октреотид», «Сандостатин»;
- ингибиторы ароматазы - «Аромазин», «Эгистразол», «Эстролет»;
- противосудорожные препараты - «Глюконат кальция», «Хлористый кальций».
Для успешного выведения избытка фосфора из организма хорошо зарекомендовал себя ежедневный гемодиализ.
Хирургическое лечение проводится при акромегалии. Также оно показано больным с прогрессирующим ухудшением зрения, выраженным болевым синдромом и серьезными увечьями. Для исправления врожденных или приобретенных дефектов костей проводят костную пластику. Опухоль или кисту из кости выскабливают, не затрагивания здоровые ткани.
Профилактика
Профилактика заключается в следующем: люди с такой патологией должны регулярно делать физические упражнения, чтобы укреплять мускулатуру; если женщина хочет забеременеть, тогда ей необходимо проконсультироваться с гинекологом и генетиком. Такая патология диагностируется у одного человека на один миллион жителей планеты. К сожалению, на сегодняшний день еще нет специфической терапии. Существует лишь симптоматическое лечение. Но если пациент будет находиться под контролем врача, есть шанс на благоприятный исход.
В середине ХХ столетия американский ученый Фуллер Олбрайт открыл новое редчайшее наследственное заболевание, поражающее костные ткани и кожные покровы, замедляющее умственное и физическое развитие человека. Позже редкой болезни было присвоено научное название псевдогипопаратиреоз. За всю историю изучения симптома Олбрайта в мировой медицине было зафиксировано лишь около 300 случаев болезни. При этом с неприятным диагнозом гораздо чаще приходилось сталкиваться представительницам женского пола.
Почему возникает синдром
Псевдогипопаратиреоз – редкая патология, передающаяся по наследству. По своим проявлениям данное заболевание имеет сходство с гипопаратиреозом. Однако в случае с симптомом Олбрайта, болезнь проявляется не в результате снижения функций паращитовидных желез, а из-за нарушений чувствительности тканей к действию паратгормона при его достаточном уровне секреции. Данное нарушение провоцирует изменение уровня кальция и фосфора в организме больного. В результате возникают проблемы с формированием костной ткани, а также процессом выработки гормонов.
Наследование синдрома Олбрайта происходит по линии X-хромосом. Именно поэтому количество женщин, столкнувшихся с заболеванием, в два раза превышает число мужчин. Также доказано, что болезнь не наследуется от отца к сыну.
Симптомы болезни
Симптоматика болезни зависит от клеточного расположения мутировавшего гена. Заболевание может проявить себя как в раннем возрасте, так и в более зрелые годы. Главным признаком патологии станет отставание в физическом и умственном развитии. Кроме того, можно выделить три сопутствующих признака, по которым можно определить заболевание:
- Ранее половое созревание. У девочек обильные и болезненные менструации приходят в детском возрасте. Даже в младенчестве у детей могут проявиться вторичные половые признаки: у девочек начинают развиваться молочные железы, у мальчиков могут появиться кисты яичков и усиленный рост волос в области гениталий.
- Поражение кожных покровов, проявляющееся в гиперпигментации. На теле возникают желто-коричневые пятна, имеющие неровные края. Локализация может наблюдаться в самых разных местах: в грудной области, на спине, в зоне поясницы, на бедрах и ягодицах. Если болезнь передалась по наследству, то светло-коричневые пятна появляются у ребенка с рождения.
- Фиброзная остеодисплазия, которую характеризует ускоренный рост и окостенение скелета. В результате кости человека деформируются, приобретают ассиметричный вид. Часто это приводит к искривлению позвоночника, хромоте. Однако через некоторое время рост резко замедляется, и человек, страдающий синдромом Олбрайта, остается низкорослым даже во взрослом возрасте. Чаще всего к этой проблеме добавляется еще и избыточный вес.
Псевдогипопаратиреоз может сопровождаться и другими заболеваниями эндокринной системы – , гипотиреозом или гипертиреозом, гинекомастией.
Диагностика заболевания
Чаще всего синдром Олбрайта диагностируется у детей 5-10 лет. Именно в этом возрасте наиболее полно прослеживается специфическая картина заболевания.
Кроме визуального осмотра пациента, для диагностирования болезни во врачебной практике применяются:
- генетическое исследование;
- рентгенодиагностика, позволяющая выявить отклонения в формировании скелета и костной ткани;
- лабораторные анализы на гормоны;
- анализ крови, определяющий уровень содержания фосфора и кальция;
- УЗИ органов малого таза (для представительниц женского пола), позволяющее определить отклонения в работе яичников.
В дополнение к основным исследованиям также проводится тест на фосфаты и ЦАМФ в моче. Он сдается через 4 часа после предварительного внутривенного введения паратгормона в кровь. Если показатели в моче при этом не изменяется, значит, ткани почек являются устойчивыми к гормону. Таким образом, диагноз окончательно подтверждается.
Лечение синдрома Олбрайта
Главная задача врача, поставившего диагноз «псевдогипопаратиреоз», заключается в том, чтобы поддерживать в норме концентрацию кальция в крови пациента. Для этих целей будут назначены специальные лекарственные препараты, дозировку которых определит специалист. Чтобы усвоение кальция проходило легче, пациенту также назначается прием витамина Д.
Больному придется соблюдать диету, прописанную врачом и ограничивающую прием продуктов, содержащих фосфор.
Когда синдром Олбрайта сопровождается дополнительными эндокринными заболеваниями, дополнительно может быть прописана заместительная гормональная терапия.
Если пациенту будет назначена грамотное комплексное лечение, то прогнозы жизни могут быть весьма благоприятными. Однако больным, столкнувшимся с редким генетическим нарушением, стоит знать, что полностью излечить дефект и устранить последствия его проявления на сегодняшний день невозможно. Для того чтобы заболевание не передалось по наследству, пациентам следует регулярно посещать консультации врачей-генетиков.